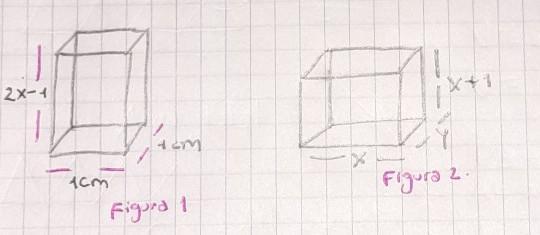
hallar el volumen de los cuerpos (los factores laterales se dejan indicados)
-
Materia:
Matemáticas -
Autor/a:
angelique -
Creada:
hace 1 año
Respuestas 1
Respuesta:
base por altura la del rectángulo y el cuadrado es la suma de todos los lados
-
Autor/a:
crumblesupuw
-
Califica una respuesta:
3
¿Conoces la respuesta? Añádela aquí
Escoger idioma y región
How much to ban the user?
1 hour
1 day
100 years